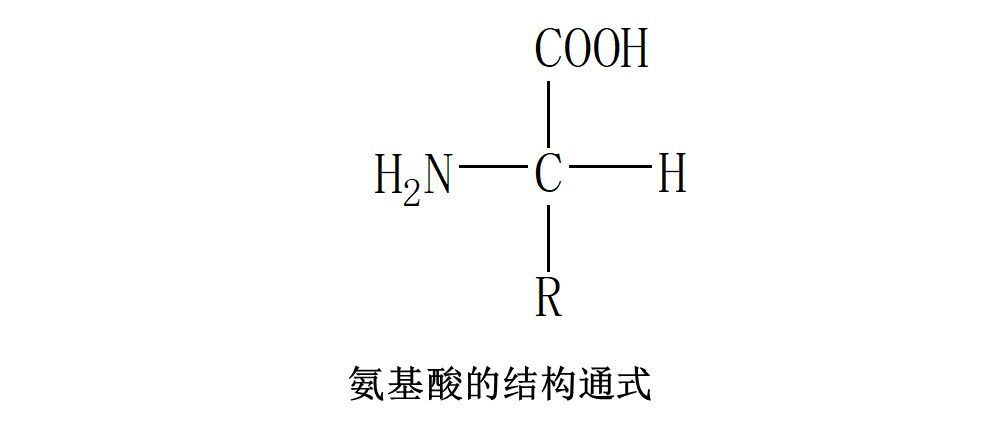食品生物化学期末梳理
梳理(实际上是按复习ppt照抄)
糖
- 多羟基的醛或多羟基的酮及其缩合物、衍生物的总称。
- 多羟基可以增强单糖的水溶性
- 单糖:葡萄糖、果糖、半乳糖
- 双糖:麦芽糖(葡萄糖+葡萄糖)、蔗糖(果糖+葡萄糖)、乳糖(半乳糖+葡萄糖)
- 多糖:淀粉(葡萄糖组成)、纤维素(葡萄糖组成)、糖原(葡萄糖组成)、果胶(杂多糖)
- 葡萄糖属于六碳糖(己糖)、核糖属于五碳糖(戊糖)
- 葡萄糖属于醛糖,果糖属于酮糖
- 甜度是以蔗糖的甜度为参考进行比较,蔗糖的甜度为1。
- 淀粉遇到碘变蓝色。
- 糖原分为肌糖原和肝糖原,存在于动物中。
- 纤维素存在于植物中。
- 美拉德反应:羰基和氨基经过缩合、聚合反应生成类黑色素的反应。
- 淀粉糊化:淀粉在适当温度下吸水膨胀形成均匀糊状溶液的现象称为糊化。
- 淀粉老化:淀粉溶液经缓慢冷却或淀粉凝胶长期放置会变成不透明甚至产生沉淀,称为淀粉的老化。
- 糖的生理作用
- (1)能源物质。人体所需能量的70%来自糖的氧化。
- (2)结构成分。糖蛋白和糖脂是细胞膜的重要成分。
- (3)构成生物活性物质。糖蛋白在免疫、细胞识别、血型区分等多种生理功能中发会作用。
- (4)合成其他生物分子。如糖可以用来合成脂类、氨基酸等。
脂
相关概念
脂肪是由一个甘油和三个脂肪酸结合形成的酯
皂化值:1克油脂完全皂化时所需要的氢氧化钾的毫克数
酯值:反映油脂中甘油酯含量
酸价:表示油脂中游离脂肪酸的数量,酸价越高,游离脂肪酸越多,新鲜程度下降。
碘值:衡量脂肪的不饱和程度,碘值越高,不饱和程度越高。
过氧化值:衡量脂肪氧化初期的氧化程度
油脂的氢化:在高温、高压和金属镍催化下,油脂中的碳碳双键与氢发生加成反应,称为油脂的氢化。
不饱和脂肪酸:含有一个或多个碳碳双键的脂肪酸
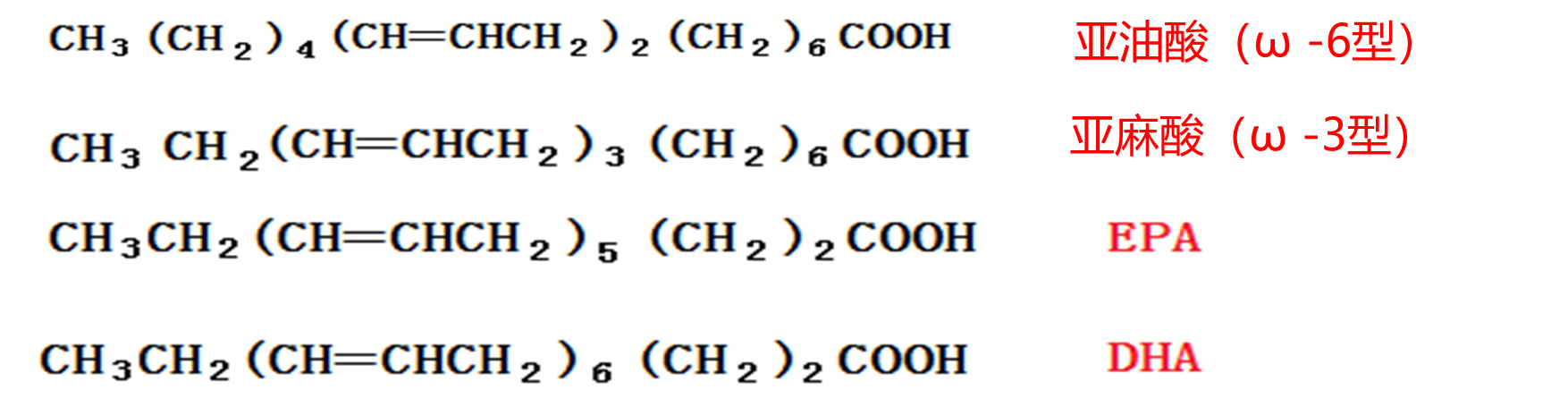
亚油酸、亚麻酸、DHA、EPA属于多不饱和脂肪酸
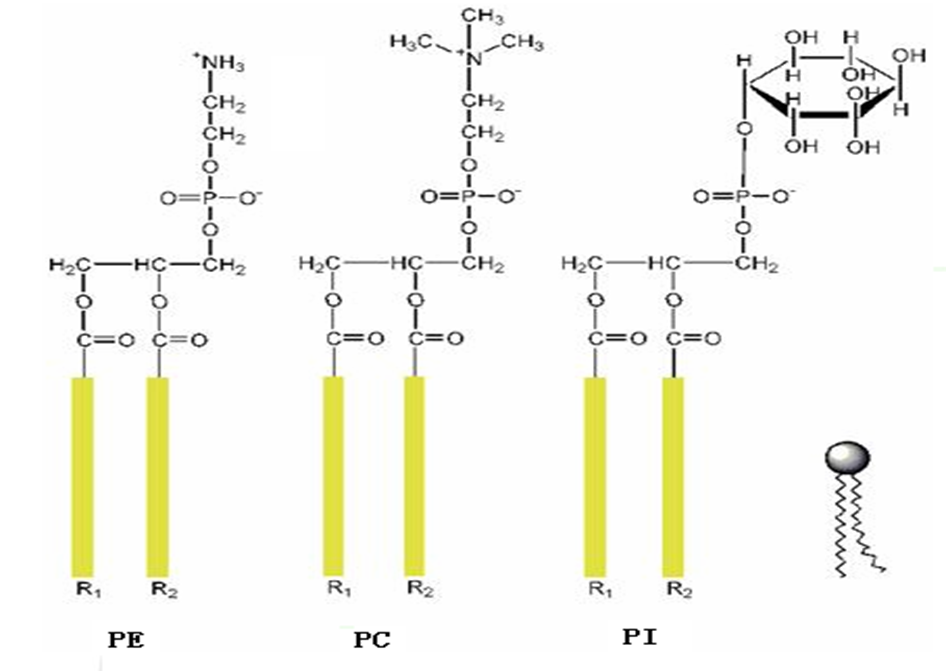
磷脂的头部具有亲水性,尾部由两条脂肪酸链组成,具有疏水性
蜡在常温下是固态,加热可成液态。
脂类的生物学意义:
(1)脂类是生物能量的主要贮存形式;
(2)脂类对生物体具有保护作用;
(3)脂类是构成生物膜的基本组成成分;
(4)脂类是生物细胞内重要的生理活性物质。
油脂的处理
油脂的制取:压榨法、熬炼法、浸出法、机械分离法。
油脂的精炼:沉降和脱胶、脱酸、脱色、脱臭。
磷脂
亚油酸、亚麻酸、DHA、EPA
蛋白质
相关概念
- 蛋白质是由氨基酸以肽键链接而成
- 必需氨基酸:赖氨酸、苯丙氨酸、蛋氨酸、亮氨酸、异亮氨酸、缬氨酸、苏氨酸、色氨酸。口诀:笨蛋来宿舍晾一晾鞋(每个老师教的不一样)
- 蛋白质系数:每测得1克氮即相当于6.25克蛋白质(100/16=6.25),6.25称为蛋白质系数。
- 氨基酸等电点:氨基酸分子所带的净电荷为零时所处的pH
颜色反应
- 水合茚三酮反应,生成蓝紫物质;
- 双缩脲反应,生成紫红色物质;
- 酚(酚酞)试剂反应,生成蓝色物质
结构
- 蛋白质的一级结构是指氨基酸的连接方式(肽键)和排列顺序。
- 蛋白质的二级结构是指蛋白质多肽链折叠和盘绕方式。
- 蛋白质的三级结构是指多肽链在二级结构的基础上进一步盘绕卷曲,形成较紧密的立体构象。
- 蛋白质的四级结构是指具有相对独立三级结构的亚基再经次级键结合而成的空间构象。
性质
- 蛋白质是高分子化合物,其相对分子质量很大,蛋白质分子直径约为1~100 nm,颗粒大小在胶体粒子的范围,故蛋白质溶液为胶体溶液。
- 蛋白质和氨基酸一样,既能和酸作用又能和碱作用,是两性电解质。当某一pH条件时,蛋白质解离成阳、阴离子的数量相等,净电荷为零,此时溶液的pH称为蛋白质等电点。等电点时蛋白质溶解度最差。 - 蛋白质在高温、高压、强酸强碱等剧烈作用下,蛋白质的理化性质发生改变,生物活性丧失,这种现象称为蛋白质的变性。
- 当蛋白质变性程度不高,可在消除变性因素条件下使蛋白质恢复或部分恢复其原有的构象和功能,称为复性。如果变性因素作用剧烈,变性过甚,不可能发生复性,称为不可逆变性。
- 蛋白质盐析:在蛋白质溶液中加入大量中性盐至饱和或半饱和程度,可以使蛋白质从溶液中沉淀析出。
生物学意义
- 结构功能:蛋白质可以作为生物体的结构成分;
- 催化功能:生物体内的酶大多数由蛋白质构成,是有机体新陈代谢的催化剂;
- 运输功能:血红细胞可以运输氧气;
- 贮存功能:某些蛋白质可以贮存氨基酸作为生物体的养料。
- 运动功能:肌肉中的肌球蛋白和肌动蛋白是运动系统的必要成分。
- 防御功能:抗体由蛋白质构成,起到免疫防御作用;
- 调节功能:某些激素和激素受体是由蛋白质组成;
- 信息传递功能:细胞膜上的糖蛋白参与信息传递过程;
- 遗传调控作用:遗传信息的贮存和表达都与蛋白质有关。
- 其他功能:某些生物能合成有毒啊的蛋白质,用于攻击和自卫。
酶
相关概念
- 酶是生物体内产生的,以蛋白质或RNA为主要成分的生物催化剂。
- 酶原:无活性的酶的前体称为酶原。
- 酶活力是指酶催化一定化学反应的能力,用在某一条件下用酶促反应速率的初速度表示
- α-淀粉酶:作用于α-1,4糖苷键,随意位置切断淀粉链;
- β-淀粉酶:作用于α-1,4糖苷键,每隔一个位置切断淀粉链;产物是麦芽糖
- 葡萄糖淀粉酶:作用于α-1,4糖苷键,逐个位置切断淀粉链;产物是葡萄糖
- 异淀粉酶(脱支酶):作用于α-1,6糖苷键;由支链淀粉变直链淀粉
酶的作用特点
(1)催化效率极高;
(2)高度的专一性;
(3)反应条件温和;
(4)活性可调节
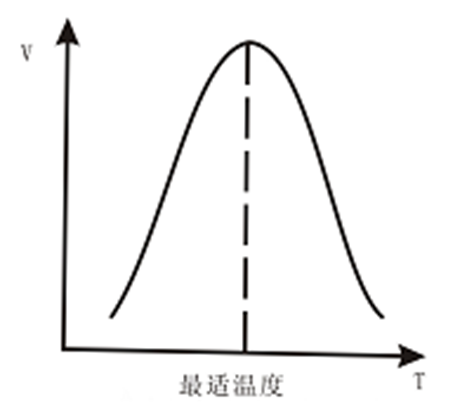
温度对酶促反应速率有双重影响:
当温度升高,反应速率加快。另一方面由于酶是蛋白质,随着温度升高而使酶逐步而失活。
核酸
相关概念
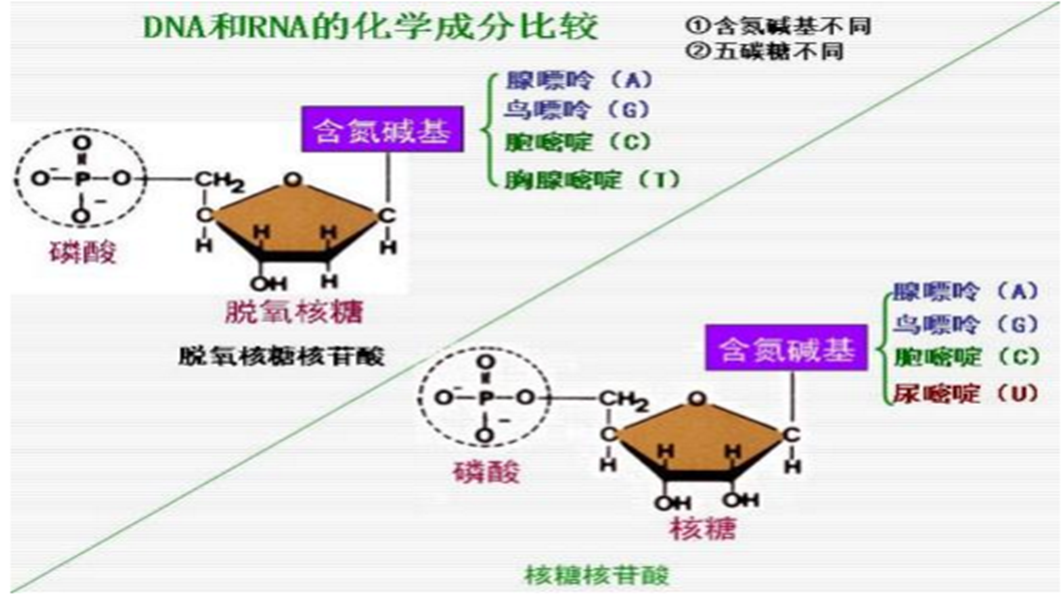
- 核酸是由核苷酸通过磷酸二酯键链接而成组成;核苷酸是由核苷和磷酸组成;核苷是由戊糖和碱基组成。
- DNA的组成单位是脱氧核糖核苷酸;
- RNA的组成单位是核糖核苷酸;
- 组成DNA的碱基是A(腺嘌呤)G(鸟嘌呤)C(胞嘧啶)T(胸腺嘧啶);
- 组成RNA的碱基是A(腺嘌呤)G(鸟嘌呤)C(胞嘧啶)U(尿嘧啶);
- DNA碱基配对原则:A-T、C-G。
核酸结构
- 核酸的一级结构指的是核苷酸的排列顺序;
- DNA的二级结构指的是双螺旋结构
核酸变性&复性
- 核酸的变性:在某些理化因素作用下(温度、酸碱、有机溶剂、尿素等),
- 核酸分子互补双链之间氢键断裂,使双螺旋结构松散变成单链的过程。
- 核酸的复性:又称退火,变性核酸在一定条件下如温度逐步恢复到生理范围内,两条互补链重新恢复天然的双螺旋构象。
核酸摄入过量导致嘌呤高导致尿酸高导致痛风
摄入含核酸丰富的食品,经消化吸收后,核酸中的嘌呤化合物经分解代谢可产生尿酸,使尿液和血液呈酸性。在一般情况下,尿酸可完全由尿排出,不在身体某些关节处存留,但对个别嘌呤代谢障碍的人,尿酸累积多了,可能会导致痛风病。
维生素
相关概念
- 维生素是维持机体正常生命活动必不可少的一类微量小分子有机物。
- 脂溶性维生素:维生素ADEK
- 水溶性维生素:维生素BC
- 机体缺少某种维生素会导致缺乏症,这是因为缺乏维生素能使物质代谢发生障碍。
- 维生素A,防夜盲症
- 维生素C,抗氧化,防败血症
- 维生素D,防软骨病或佝偻病
- 维生素E,抗氧化
维生素的特点
- 量少效高。
- 从食物中摄取。
- 调节物质。
- 缺少会患病或死亡。
水和矿物质
相关概念
自由水:是以毛细管凝聚状态存在于细胞间的水分。
结合水:存在于食品种的与非水成分通过氢键结合的水。
自由水和结合水的区别:结合水在食品中不能作为溶剂,不能被微生物利用,在-40℃时不结冰;而自由水可以作为溶剂,可以被微生物利用,在-40℃会结冰。
水份活度:表示食品中的水可以被微生物所利用的程度。
水的生理意义
(1)构成人体的重要成分;
(2)体内化学作用的介质;
(3)体内物质运输的载体;
(4)维持体温的载温体;
(5)内体摩擦的缓冲剂。
矿物质
钙:组成骨骼和牙齿,抑制肌肉兴奋性;钙容易与植物种的植酸、草酸等形成不溶性的盐,导致钙的吸收率降低;吃肉蛋奶可以补充钙
磷:组成骨骼和牙齿;
碘:参与甲状腺素的合成,与体力和智力发育有关;小孩缺碘容易换呆小症
铁:参与组成血红蛋白,参与氧的运输;摄入内脏和红肉可以补充铁元素
代谢
生物体内主要的呼吸链有2条,分别是NADH+H+和FADH2,最终产物是水。
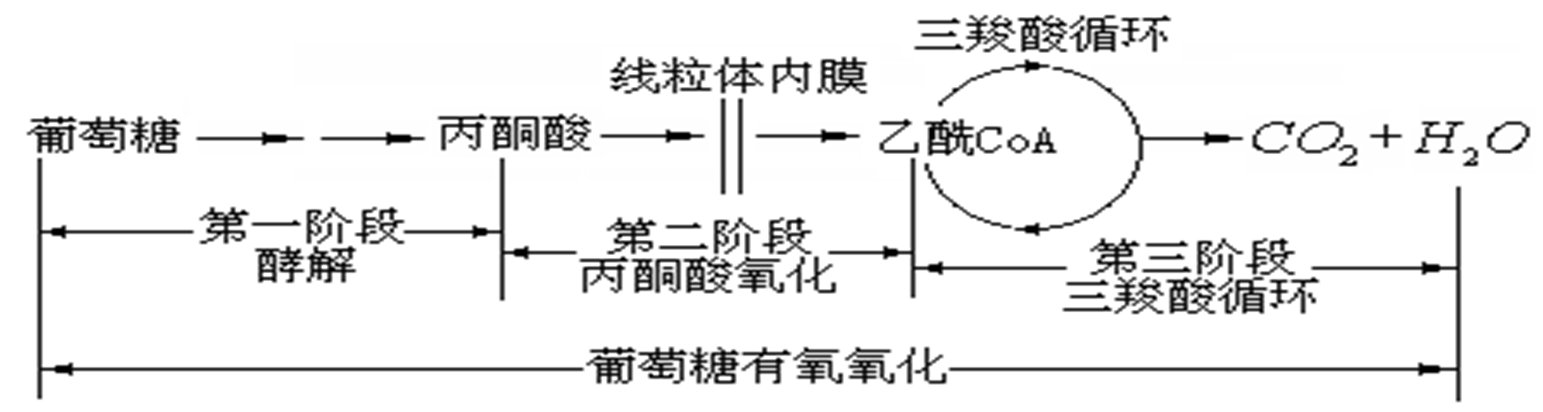
EMP糖酵解途径的产物是丙酮酸。
TCA循环发生在线粒体内 (三羧酸循环)